Saúde
O antibiótico mais importante do mundo tornou-se o nosso maior desafio
Hoje, no 80º aniversário da atribuição do Prêmio Nobel pela descoberta e desenvolvimento da penicilina, o Dr. Alistair Farley , Líder Científico do Instituto Ineos Oxford para Pesquisa Antimicrobiana (IOI), defende que a...
Quarta-feira (10 de dezembro) comemora-se o 80º aniversário da atribuição do Prêmio Nobel pela descoberta e desenvolvimento da penicilina. Crédito da imagem: sprng23, Getty Images.
Nesta quarta-feira (10), no 80º aniversário da atribuição do Prêmio Nobel pela descoberta e desenvolvimento da penicilina, o Dr. Alistair Farley , Líder Científico do Instituto Ineos Oxford para Pesquisa Antimicrobiana (IOI), defende que a colaboração por trás dessa conquista seja novamente canalizada para enfrentar um dos maiores desafios médicos globais da nossa época.
Dr. Alistair Farley. Crédito: The IOI.
Em 10 de dezembro de 1945, Alexander Fleming, Howard Florey e Ernst Chain receberam conjuntamente o Prêmio Nobel de Fisiologia ou Medicina " pela descoberta da penicilina e seu efeito curativo em diversas doenças infecciosas ".
A descoberta da penicilina e sua subsequente produção industrial durante a Segunda Guerra Mundial são justamente consideradas um dos maiores avanços médicos do século XX . A penicilina desempenhou um papel fundamental para milhões de soldados aliados e, nos últimos 80 anos, salvou centenas de milhões de vidas.
O desenvolvimento da penicilina estabeleceu um novo modelo para a pesquisa translacional. A descoberta da penicilina por Fleming, a partir do fungo Penicillium , foi publicada como uma observação curiosa. Com base nessas descobertas, Florey, Chain e Norman Heatley, da Escola de Patologia Dunn, em Oxford, isolaram a penicilina pela primeira vez , utilizando comadres para o cultivo e fermentação do fungo. Embora as quantidades de penicilina pura fossem limitadas, foram suficientes para demonstrar seus efeitos curativos em camundongos e em um paciente humano. O programa da penicilina foi posteriormente financiado por uma bolsa da Fundação Rockefeller e, em seguida, pela participação de empresas farmacêuticas britânicas e americanas, com o apoio de seus governos. Isso levou, de forma notavelmente rápida, à produção em massa de penicilina, em um dos primeiros exemplos de colaboração transatlântica para a pesquisa biomédica.
A era de ouro dos antibióticos e o aumento da resistência
O desenvolvimento da penicilina anunciou uma era de descobertas incrivelmente produtivas de antibióticos e avanços médicos. Infecções como gonorreia e pneumonia, que antes eram fatais ou gravemente debilitantes, tornaram-se tratáveis, e avanços possibilitados por antibióticos ocorreram em diversas áreas da medicina, como cirurgia, medicina de trauma e tratamento do câncer. A maioria das classes de antibióticos em uso hoje foi identificada entre aproximadamente 1940 e 1965, na era de ouro dos antibióticos.
"O desenvolvimento da penicilina anunciou uma era de descobertas incrivelmente produtivas de antibióticos e avanços médicos. Infecções que antes eram fatais ou gravemente debilitantes passaram a ser tratáveis, e descobertas revolucionárias possibilitadas por antibióticos ocorreram em diversas áreas da medicina."
Assim como todos os organismos vivos, as bactérias evoluem e se adaptam às pressões seletivas, e houve relatos crescentes de resistência a antibióticos durante esse período (agora conhecida como resistência antimicrobiana, RAM).
De fato, em seu discurso de aceitação do Prêmio Nobel, Fleming alertou sobre os perigos do uso de quantidades subletais de penicilina, pois isso levaria ao desenvolvimento de bactérias resistentes a esse antibiótico. As bactérias podem se adaptar, por exemplo, impedindo a entrada dos medicamentos nas células ou bombeando os medicamentos para fora das células por meio de bombas de efluxo. O alvo do antibiótico na bactéria também pode ser modificado, reduzindo a eficácia do medicamento, ou a bactéria pode produzir enzimas degradantes, como as -lactamases, que destroem o antibiótico antes que ele atinja seu alvo.
Diversos fatores promovem a resistência antimicrobiana (RAM), incluindo o baixo custo e a prescrição excessiva de antibióticos, o término precoce dos tratamentos, a falta de higiene e saneamento básicos em muitos países de baixa e média renda e o uso de antibióticos como promotores de crescimento na produção pecuária.
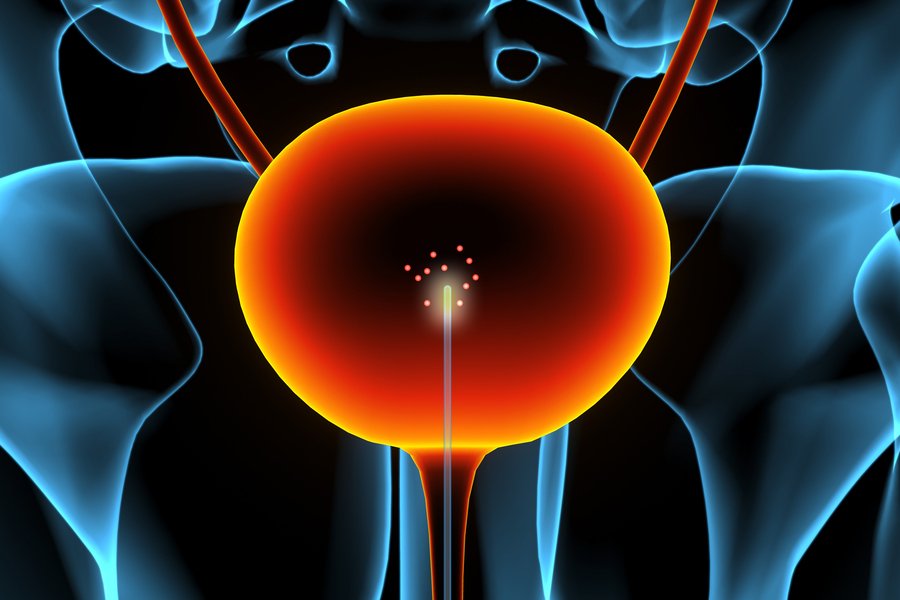
Hoje, prevê-se que a resistência antimicrobiana (RAM) cause 39 milhões de mortes até 2050, se não for combatida, contribuindo para uma perda do PIB de US$ 1 a 3,4 trilhões por ano até 2030. No entanto, já estamos testemunhando os impactos devastadores da RAM ao nosso redor. Em 2023, uma em cada seis infecções bacterianas no mundo era resistente a antibióticos, e houve 4,71 milhões de mortes associadas à RAM em 2021. O fardo da RAM afeta desproporcionalmente os países de baixa e média renda; bebês na Nigéria são rapidamente colonizados por bactérias multirresistentes em seus intestinos, e os antibióticos estão se tornando cada vez mais ineficazes no tratamento de doenças comuns, como infecções do trato urinário.
Descobrindo a próxima geração de antibióticos
Placa azul na Escola de Patologia Dunn. Crédito: Owen Massey McKnight.
Desde 2017, apenas 12 antibióticos foram aprovados , dez dos quais pertencem a classes de medicamentos já existentes que apresentam mecanismos de resistência conhecidos em patógenos. Para agravar essa falta de inovação, a maioria das empresas farmacêuticas não está mais pesquisando e desenvolvendo ativamente novos antibióticos, em parte devido a falhas de mercado e baixos retornos comerciais iniciais.
Aqui no IOI, estamos desenvolvendo novos antibióticos e encontrando maneiras inovadoras de prolongar a vida útil dos já existentes.
Coletamos amostras bacterianas de regiões do mundo onde a resistência é maior e analisamos seus genes e mecanismos de resistência. Esses dados orientam nosso processo de descoberta de fármacos, desde a identificação do alvo até o desenvolvimento de candidatos. As amostras nos permitem testar nossos antibióticos em desenvolvimento diretamente em isolados resistentes a medicamentos contemporâneos e desenvolver fármacos eficazes em regiões do mundo com as maiores taxas de resistência.
Nós somos:
Desenvolver novos compostos, também conhecidos como inibidores, que bloqueiem os mecanismos de resistência em bactérias resistentes a medicamentos.
Desenvolver novas combinações de antibióticos existentes para aumentar sua eficácia.
Projetar e desenvolver a próxima geração de antibióticos à base de penicilina.
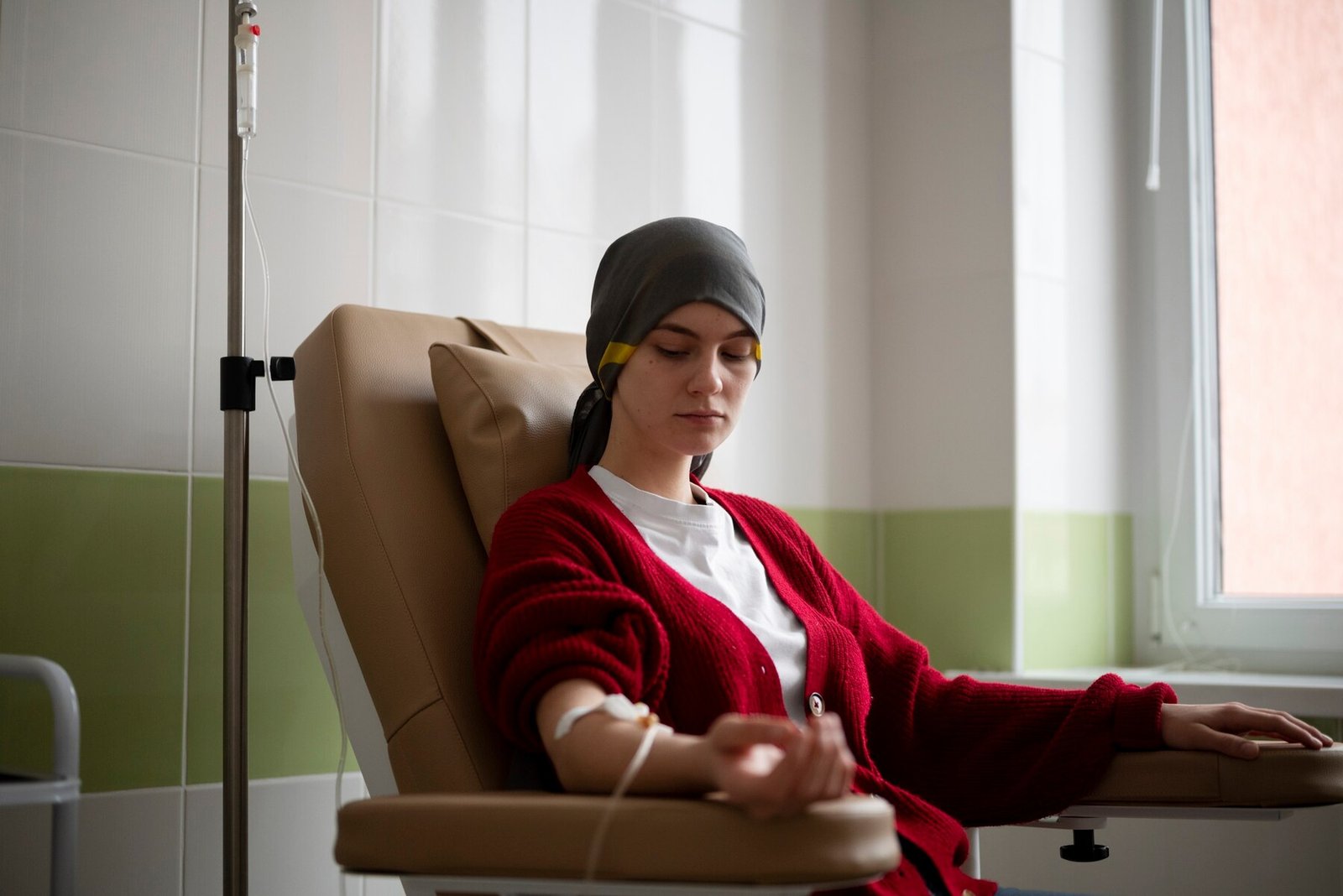
Nosso objetivo é desenvolver novos antibióticos para infecções e doenças como infecções da corrente sanguínea e infecções complicadas do trato urinário, bem como tuberculose, que estão se tornando cada vez mais difíceis de tratar.
As próximas fronteiras no combate à resistência antimicrobiana.
"A maioria das empresas farmacêuticas já não investe ativamente em pesquisa e desenvolvimento de novos antibióticos, em parte devido a falhas de mercado e baixos retornos comerciais iniciais."
O desenvolvimento de novos antibióticos é vital, mas não pode ser a única solução para a resistência antimicrobiana. A resistência é, em grande parte, uma resposta natural ao uso de antibióticos. Com o tempo, mesmo os antibióticos mais recentes e eficazes perderão sua eficácia, a menos que também mudemos a forma como os utilizamos e gerenciamos.
Combater essa ameaça exige um esforço interdisciplinar e global. A resistência antimicrobiana afeta todos os 17 Objetivos de Desenvolvimento Sustentável (ODS) da ONU , impactando desproporcionalmente as populações mais vulneráveis. Precisamos de um uso mais racional de antibióticos, testes diagnósticos rápidos, acessíveis e confiáveis, saneamento básico aprimorado e (quando apropriado) vacinação preventiva eficaz.
Mais de 200 pesquisadores da Universidade de Oxford estão combatendo a resistência antimicrobiana a partir de abordagens diferentes, porém interconectadas:
Um grupo de pesquisadores da Oxford Martin School está desenvolvendo testes rápidos que podem identificar espécies bacterianas e determinar a quais antibióticos elas são suscetíveis, em apenas 30 minutos.
Pesquisadores do Departamento de Engenharia desenvolveram um novo sistema de administração de medicamentos que utiliza nanopartículas ativadas por ultrassom para destruir biofilmes bacterianos. Isso oferece uma solução promissora para pacientes que sofrem de infecções crônicas resistentes a antibióticos.
A Unidade de Pesquisa em Medicina Tropical Mahidol Oxford (MORU) está apoiando um projeto no Camboja que utiliza as artes circenses para conscientizar a comunidade sobre o uso adequado de antibióticos.
Uma equipe de microbiologistas do IOI está trabalhando com profissionais de saúde em 28 hospitais e clínicas em 7 países para melhorar o tratamento de infecções da corrente sanguínea, incluindo sepse.
"O desenvolvimento de novos antibióticos é vital, mas não pode ser a única solução para a resistência antimicrobiana... Com o tempo, mesmo os antibióticos mais recentes e eficazes perderão sua eficácia, a menos que também mudemos a forma como os utilizamos e gerenciamos."
Ao celebrarmos e refletirmos sobre o 80º aniversário da atribuição do Prêmio Nobel à penicilina, devemos canalizar a urgência e a colaboração demonstradas pela equipe da penicilina, integrando as novas tecnologias disponíveis para enfrentarmos um dos problemas mais prementes que a saúde humana enfrenta.
A sinergia internacional entre universidades, indústria, filantropia e governo foi crucial para transformar a observação de Fleming em um medicamento inovador produzido em massa. Devemos continuar os esforços de colaboração global e dar continuidade ao legado da penicilina. O custo de não fazê-lo nos levará a uma era pós-antibiótica com profundas consequências para todos nós.
Para obter mais informações sobre esta notícia ou para republicar este conteúdo, entre em contato com news.office@admin.ox.ac.uk