Saúde
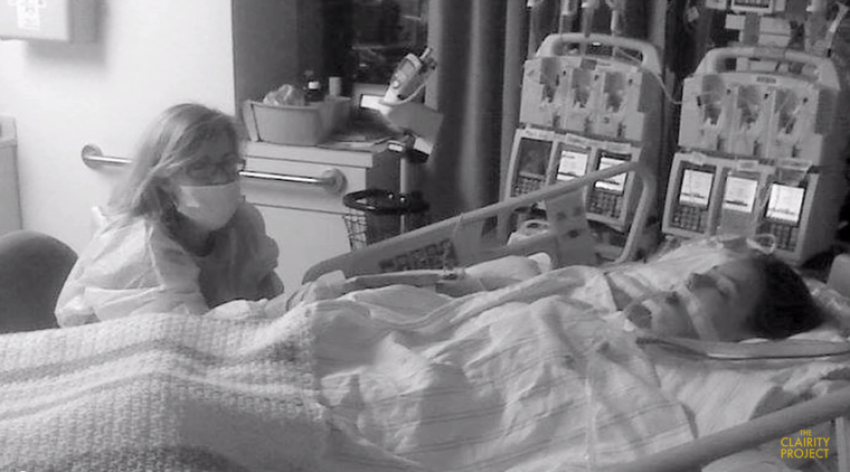
Células do próprio cérebro podem ser reprogramadas para restaurar movimentos, aponta estudo
Pesquisa liderada por Harvard identifica caminho para regenerar neurônios motores destruídos por lesões na medula e doenças como esclerose lateral amiotrófica.
Identificação e cultura de progenitores corticais SOX6+/NG2+ com alta pureza e fidelidade.
( A ) Micrografia confocal do neocórtex de camundongo no dia pós-natal 7 (P7) mostrando a expressão de SOX6 por um subconjunto de células proliferativas BrdU+. Veja também a Figura 1—Figura Suplementar 1. ( B ) Hibridização in situ de Neurog2 no córtex de camundongos Sox6 selvagens (wt) (esquerda) e knockout (KO) (direita) em P6. ( B' ) Insets mostrando as áreas delimitadas em B. A perda de Sox6 resulta em expressão ectópica generalizada de Neurog2 ( B' )...
Um grupo internacional de cientistas identificou um método inédito para transformar células de suporte do cérebro adulto em neurônios motores altamente especializados — os chamados neurônios corticoespinais, responsáveis pelo controle dos movimentos voluntários. A descoberta, publicada nesta semana na revista científica eLife, abre novas perspectivas para o tratamento de lesões na medula espinhal e de doenças neurodegenerativas como a esclerose lateral amiotrófica (ELA).
O estudo foi liderado por pesquisadores da Universidade Harvard, em colaboração com a Koç University, da Turquia, e centros de pesquisa da Califórnia. Pela primeira vez, cientistas conseguiram induzir células progenitoras presentes no córtex cerebral adulto — tradicionalmente consideradas incapazes de gerar neurônios — a se diferenciar em neurônios corticoespinais funcionais, com características morfológicas, moleculares e elétricas semelhantes às encontradas no cérebro humano saudável.
“Conseguimos acionar um programa genético latente nessas células, levando-as a se tornarem neurônios altamente específicos, em vez de células genéricas”, afirma Jeffrey D. Macklis, professor do Departamento de Biologia de Células-Tronco e Medicina Regenerativa de Harvard e autor sênior do trabalho.
Um gargalo histórico da neurologia
Os neurônios corticoespinais — também chamados de neurônios motores superiores — são essenciais para funções como caminhar, escrever e realizar movimentos finos. Eles degeneram precocemente na ELA e têm seus axônios rompidos em traumas da medula espinhal. Apesar de décadas de pesquisa, não existiam até agora modelos laboratoriais confiáveis para estudar a perda seletiva dessas células ou tentar regenerá-las.
Segundo a Organização Mundial da Saúde, lesões medulares afetam entre 250 mil e 500 mil pessoas por ano no mundo, enquanto a ELA atinge cerca de 2 a cada 100 mil indivíduos anualmente. Em ambos os casos, a perda dos neurônios corticoespinais leva a déficits motores graves e irreversíveis.
“Esse tipo de neurônio sempre foi um ‘calcanhar de Aquiles’ da neurociência experimental”, diz Abdulkadir Ozkan, primeiro autor do estudo. “Não havia como reproduzi-lo com fidelidade em laboratório, o que limitava tanto a compreensão da doença quanto o desenvolvimento de terapias”.
Engenharia genética precisa
A equipe identificou que um subconjunto de células progenitoras do cérebro adulto, conhecidas como SOX6+/NG2+, mantém um potencial neurogênico adormecido. Usando uma combinação específica de fatores genéticos — que ativam programas neuronais e bloqueiam o destino glial dessas células — os pesquisadores conseguiram induzir a formação de neurônios com um único axônio longo, marca registrada dos neurônios corticoespinais.
Os neurônios induzidos por NVOF são eletricamente ativos e possuem correntes sinápticas espontâneas.
( A–B ) Imagens representativas em alta magnificação de neurônios induzidos por NVOF no 14º dia pós-transplante (GFP pseudocolorido) com e sem cocultura de neurônios primários do prosencéfalo e meio condicionado por astrócitos. (A'-B')...
Em testes laboratoriais, cerca de 70% das células reprogramadas adquiriram morfologia neuronal em uma semana, e mais da metade passou a expressar marcadores moleculares clássicos desses neurônios. Registros eletrofisiológicos mostraram que elas eram capazes de disparar potenciais de ação e formar conexões sinápticas, sinais inequívocos de funcionalidade.
“O grau de fidelidade que observamos foi surpreendente”, afirma Hari K. Padmanabhan, coautor do estudo. “Essas células não apenas se parecem com neurônios corticoespinais — elas se comportam como tais.”
Especialistas afirmam que o trabalho representa um marco na medicina regenerativa do sistema nervoso central, um campo historicamente marcado por frustrações. Diferentemente de abordagens baseadas em transplante de células-tronco, a estratégia proposta utiliza células já presentes no cérebro, reduzindo riscos de rejeição e problemas de integração.
“A possibilidade de reprogramar células locais diretamente no cérebro muda o paradigma”, diz Macklis. “Ainda estamos longe da aplicação clínica, mas este estudo estabelece uma base sólida para terapias futuras.”
Os autores destacam que novos desafios permanecem, como demonstrar a eficácia do método em organismos vivos e garantir que os neurônios regenerados se conectem corretamente às redes existentes. Ainda assim, o avanço reacende a expectativa de que doenças antes consideradas irreversíveis possam, no futuro, ser tratadas com estratégias de regeneração neuronal personalizada.
Mais sobre o artigo
Abdulkadir OzkanHari, K Padmanabhan, Seth L Shipman Eiman Azim, Priyanka Kumar, Cameron Sadegh, Um Nazli Basak, Jeffrey D Macklis. Departamento de Células-Tronco e Biologia Regenerativa e Centro de Ciências do Cérebro, Universidade de Harvard, Estados Unidos ; Centro de Pesquisa em Medicina Translacional da Faculdade de Medicina da Universidade Koç, Turquia
Artigo publicadas pela eLife - 27 de janeiro de 2026 - https://doi.org/10.7554/eLife.100340.3