Saúde
O circuito cerebral necessário para incorporar novas informações pode estar ligado à esquizofrenia
As disfunções nesse circuito podem ajudar a explicar por que algumas pessoas com esquizofrenia perdem o contato com a realidade.
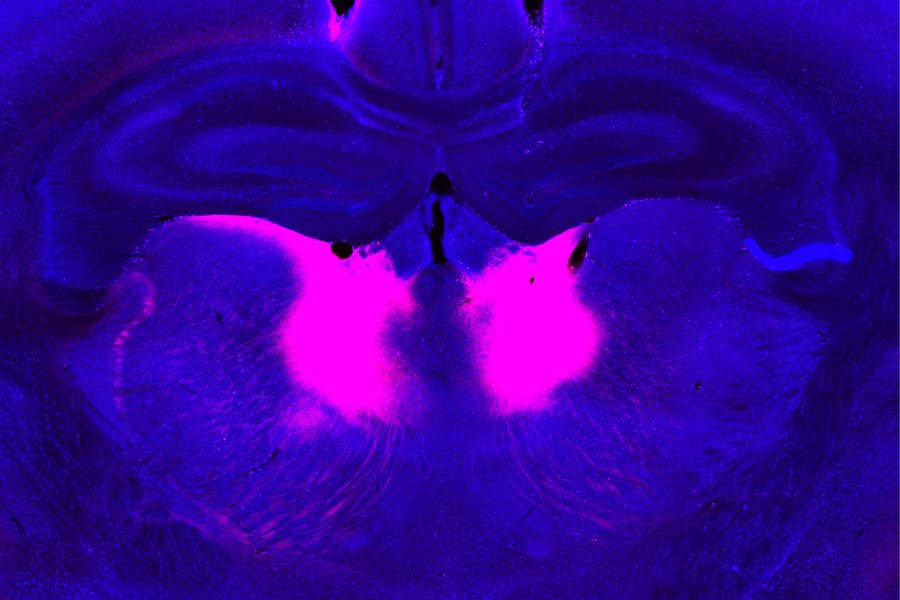
Pesquisadores do MIT identificaram neurônios no tálamo mediodorsal (marcados em rosa) cuja disfunção pode levar a prejuízos na capacidade de atualizar crenças com base em novas informações. Crédito: Cortesia dos pesquisadores
Um dos sintomas da esquizofrenia é a dificuldade em assimilar novas informações sobre o mundo. Isso pode levar pessoas com esquizofrenia a terem dificuldades para tomar decisões e, eventualmente, a perderem o contato com a realidade.
Neurocientistas do MIT identificaram uma mutação genética que parece causar esse tipo de dificuldade. Em um estudo com ratos, os pesquisadores descobriram que o gene mutado prejudica o funcionamento de um circuito cerebral responsável por atualizar crenças com base em novas informações.
Essa mutação, em um gene chamado grin2a, foi originalmente identificada em uma triagem em larga escala de pacientes com esquizofrenia. O novo estudo sugere que medicamentos que atuam nesse circuito cerebral podem ajudar a tratar alguns dos déficits cognitivos observados em pessoas com esquizofrenia.
“Se esse circuito não funcionar bem, você não consegue integrar informações rapidamente”, diz Guoping Feng, professor James W. e Patricia T. Poitras de Ciências Cerebrais e Cognitivas no MIT, membro do Broad Institute de Harvard e do MIT e diretor associado do Instituto McGovern de Pesquisa Cerebral do MIT. “Estamos bastante confiantes de que esse circuito é um dos mecanismos que contribuem para o comprometimento cognitivo, que é uma parte importante da patologia da esquizofrenia.”
Feng e Michael Halassa, professor de psiquiatria e neurociência e diretor de pesquisa translacional na Escola de Medicina da Universidade Tufts, são os autores seniores do novo estudo, publicado hoje na Nature Neuroscience . Tingting Zhou, pesquisadora do Instituto McGovern, e Yi-Yun Ho, ex-pós-doutoranda do MIT, são os autores principais do artigo.
Adaptando-se a novas informações
Sabe-se que a esquizofrenia tem um forte componente genético. Para a população em geral, o risco de desenvolver a doença é de cerca de 1%, mas sobe para 10% para aqueles que têm um dos pais ou um irmão com a doença e para 50% para pessoas que têm um gêmeo idêntico com a doença.
Pesquisadores do Centro Stanley de Pesquisa Psiquiátrica do Instituto Broad identificaram mais de 100 variantes genéticas ligadas à esquizofrenia, utilizando estudos de associação genômica ampla. No entanto, muitas dessas variantes estão localizadas em regiões não codificantes do genoma, o que dificulta a compreensão de como elas podem influenciar o desenvolvimento da doença.
Mais recentemente, pesquisadores do Centro Stanley utilizaram uma estratégia diferente, conhecida como sequenciamento de exoma completo, para revelar mutações genéticas ligadas à esquizofrenia. Essa técnica sequencia apenas as regiões codificadoras de proteínas do genoma, podendo assim revelar mutações localizadas em genes já conhecidos.
Utilizando essa abordagem em cerca de 25.000 sequências de pessoas com esquizofrenia e 100.000 sequências de indivíduos do grupo de controle, os pesquisadores identificaram 10 genes cujas mutações aumentam significativamente o risco de desenvolver esquizofrenia.
No novo estudo publicado na Nature Neuroscience , Feng e seus alunos criaram um modelo de camundongo com uma mutação em um desses genes, o grin2a. Esse gene codifica uma proteína que faz parte do receptor NMDA — um receptor ativado pelo neurotransmissor glutamato e frequentemente encontrado na superfície dos neurônios.
Zhou então investigou se esses camundongos exibiam algum dos comportamentos característicos observados em pessoas com esquizofrenia. Esses indivíduos apresentam muitos sintomas complexos, incluindo psicoses como alucinações e delírios (perda de contato com a realidade). Esses sintomas são difíceis de estudar em camundongos, mas é possível estudar sintomas relacionados, como a dificuldade em interpretar novos estímulos sensoriais.
Nas últimas duas décadas, pesquisadores da esquizofrenia têm levantado a hipótese de que a psicose pode ter origem em uma capacidade prejudicada de atualizar crenças com base em novas informações.
“Nosso cérebro pode formar uma crença prévia sobre a realidade e, quando um estímulo sensorial chega ao cérebro, um cérebro neurotípico pode usar esse novo estímulo para atualizar a crença prévia. Isso nos permite gerar uma nova crença que se aproxima da realidade”, diz Zhou. “O que acontece com pacientes esquizofrênicos é que eles se apegam demais à crença prévia. Eles não usam tantos estímulos atuais para atualizar o que acreditavam antes, então a nova crença fica distante da realidade.”
Para estudar isso, Zhou projetou um experimento no qual os ratos precisavam escolher entre duas alavancas para obter uma recompensa alimentar. Uma alavanca oferecia baixa recompensa — os ratos tinham que pressioná-la seis vezes para receber uma gota de leite. A alavanca de alta recompensa liberava três gotas a cada pressão.
No início do estudo, todos os ratos aprenderam a preferir a alavanca de alta recompensa. No entanto, à medida que o experimento prosseguia, o número de pressionamentos necessários para obter a recompensa maior aumentava gradualmente, enquanto não houve alterações na alavanca de baixa recompensa.
À medida que o esforço exigido aumentava, os ratos saudáveis começavam a alternar entre as duas alavancas. Quando precisavam pressionar a alavanca de alta recompensa cerca de 18 vezes para obter três gotas de leite, tornando o esforço por gota aproximadamente o mesmo para cada alavanca, eles eventualmente passaram a usar permanentemente a alavanca de baixa recompensa. No entanto, os ratos com uma mutação no gene grin2a apresentaram um padrão de comportamento diferente. Eles passaram mais tempo alternando entre as duas alavancas e fizeram a transição para o lado de baixa recompensa muito mais tarde.
“Descobrimos que os animais neurotípicos tomam decisões adaptativas nesse ambiente em constante mudança”, diz Zhou. “Eles conseguem alternar entre o lado de alta recompensa e o lado de baixa recompensa em torno do ponto de igualdade de valores, enquanto que, para os animais com a mutação, essa transição ocorre muito mais tarde. A tomada de decisão adaptativa deles é muito mais lenta em comparação com os animais selvagens.”
Um circuito defeituoso
Utilizando imagens de ultrassom funcional e registros elétricos, os pesquisadores descobriram que a região do cérebro mais afetada pela mutação grin2a era o tálamo mediodorsal. Essa parte do cérebro se conecta com o córtex pré-frontal para formar um circuito tálamo-cortical responsável pela regulação de funções cognitivas como o controle executivo e a tomada de decisões.
Os pesquisadores descobriram que a atividade neuronal no tálamo mediodorsal parece acompanhar as mudanças no valor das duas opções de recompensa. Além disso, os ratos apresentaram diferentes padrões de atividade neural dependendo do estado em que se encontravam — seja em um estado exploratório ou comprometidos com um dos lados.
Os pesquisadores também demonstraram que podiam usar a optogenética para reverter os sintomas comportamentais dos ratos com a mutação grin2a. Eles modificaram os neurônios do tálamo mediodorsal para que pudessem ser ativados pela luz e, quando esses neurônios foram ativados, os ratos começaram a se comportar de forma semelhante aos ratos sem a mutação grin2a.
Embora apenas uma porcentagem muito pequena de pacientes com esquizofrenia apresente mutações no gene grin2a, é possível que essa disfunção do circuito seja um mecanismo convergente de comprometimento cognitivo para um subgrupo de pacientes com esquizofrenia de causas diferentes.
Os pesquisadores afirmam que direcionar esse circuito pode oferecer uma maneira de superar alguns dos déficits cognitivos observados em pessoas com esquizofrenia. Para isso, eles estão trabalhando na identificação de alvos dentro do circuito que possam ser potencialmente alvos de medicamentos.
A pesquisa foi financiada pelos Institutos Nacionais de Saúde Mental, pelo Centro Poitras de Pesquisa de Transtornos Psiquiátricos do MIT, pelo Coletivo Yang Tan do MIT, pelo Centro K. Lisa Yang e Hock E. Tan de Terapêutica Molecular do MIT, pelo Fundo de Pesquisa da Família Stelling do MIT, pelo Centro Stanley de Pesquisa Psiquiátrica e pela Fundação de Pesquisa do Cérebro e do Comportamento.