Saúde
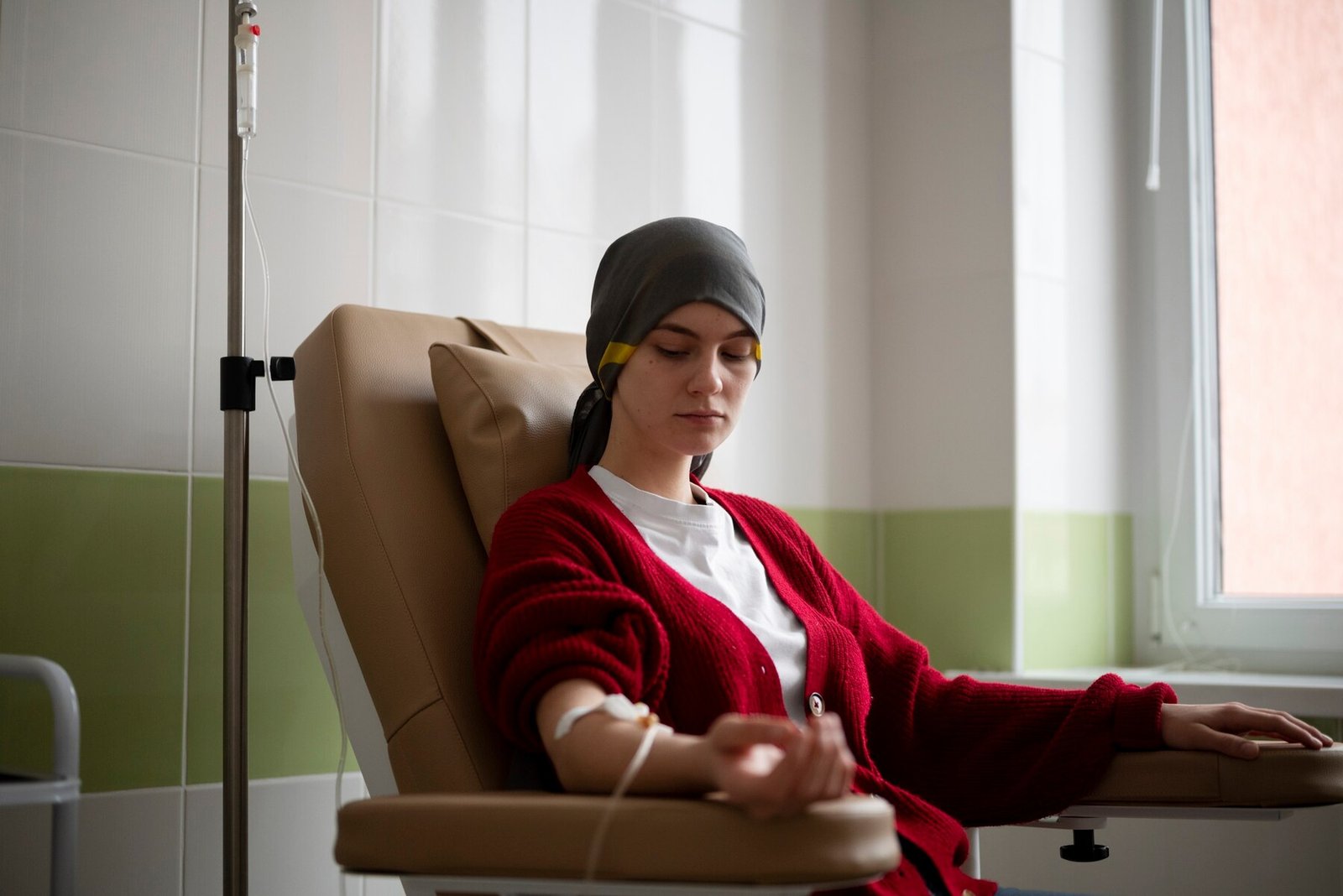
Parasita da doença do sono desafia dogma centenário e pode mudar estratégias de controle
Estudo revela que forma antes considerada 'inofensiva' do Trypanosoma brucei também infecta moscas tsé-tsé e sustenta a transmissão da doença
Imagem: Reprodução
Por décadas, a biologia do Trypanosoma brucei — o protozoário responsável pela doença do sono africana — parecia seguir um roteiro claro: apenas uma forma específica do parasita, chamada “stumpy” (curta e não proliferativa), seria capaz de infectar a mosca tsé-tsé e dar continuidade ao ciclo de transmissão. Um novo estudo publicado nesta quarta-feira (25), na revista eLife, no entanto, desafia esse paradigma ao demonstrar que a forma “slender” (longa e proliferativa) também é capaz de infectar o inseto vetor — e talvez desempenhe papel central na propagação da doença.
A pesquisa, conduzida por cientistas da Julius-Maximilians-Universität Würzburg e do Helmholtz Institute for RNA-based Infection Research, na Alemanha, foi liderada por Carina Praisler, Jaime N Lisack e o parasitologista Markus Engstler. Os resultados reforçam uma hipótese que já vinha sendo debatida na comunidade científica, mas que permanecia controversa.
“O que mostramos é que as formas slender não apenas sobrevivem no vetor, mas são plenamente capazes de completar o ciclo de vida no inseto”, afirma Engstler. “Isso muda a forma como entendemos a transmissão desses parasitas.”
Segundo o estudo, mesmo uma única célula slender pode infectar a mosca tsé-tsé, contradizendo a visão clássica de que apenas as formas stumpy — adaptadas ao ambiente do inseto — teriam essa capacidade .
Quebra de um paradigma
Historicamente, a distinção entre as duas formas do parasita era central para explicar sua biologia. As células slender se multiplicam no sangue do hospedeiro mamífero, enquanto as stumpy entram em um estado de “hibernação” celular (parada do ciclo celular) e seriam, teoricamente, as únicas aptas a sobreviver no trato digestivo da mosca.
Esse modelo, consolidado ao longo do século 20, baseava-se em observações experimentais e em características bioquímicas das formas stumpy, como a expressão da proteína PAD1 — considerada um marcador-chave de diferenciação .
No entanto, a nova pesquisa mostra que as formas slender podem ativar parte desse programa molecular sem passar por todas as etapas típicas da transformação em stumpy. Em vez disso, elas seguem uma rota alternativa, diferenciando-se diretamente na forma “procyclic”, que se desenvolve no intestino da mosca.
Dados de sequenciamento de RNA revelaram que as duas formas — slender e stumpy — permanecem “transcricionalmente distintas” durante boa parte do processo de diferenciação, convergindo apenas após cerca de 72 horas .
Evidências experimentais
Para responder a críticas anteriores, os pesquisadores realizaram uma série de experimentos rigorosos. Um dos pontos questionados era se a infecção por formas slender dependia de condições artificiais de laboratório — como o uso de compostos imunossupressores.
Os novos testes mostraram que isso não é necessário. Mesmo sem aditivos químicos, as taxas de infecção foram comparáveis: cerca de 11,6% dos insetos apresentaram infecção intestinal com suplementação e 9,2% sem ela — diferença considerada estatisticamente não significativa .
Além disso, o parasita foi capaz de infectar tanto moscas jovens quanto adultas, e tanto machos quanto fêmeas. Em moscas não jovens (não tenerais), por exemplo, as taxas de infecção no intestino médio foram praticamente idênticas entre formas slender (6,4%) e stumpy (6,6%) .
Outro dado relevante: apenas formas slender conseguiram, em alguns casos, atingir as glândulas salivares de moscas fêmeas — etapa crucial para a transmissão ao próximo hospedeiro .
O “paradoxo da transmissão”
Os resultados ajudam a resolver um enigma antigo na epidemiologia da doença do sono: o chamado “paradoxo da transmissão”. Em infecções crônicas, o número de parasitas no sangue tende a ser baixo, o que tornaria improvável que moscas ingerissem quantidades suficientes de formas stumpy para manter o ciclo da doença.
“A capacidade das formas slender de infectar a mosca oferece uma explicação elegante para esse paradoxo”, escrevem os autores . Como essas células são mais abundantes durante fases de baixa parasitemia, elas poderiam garantir a continuidade da transmissão mesmo quando as formas stumpy são raras.
A doença do sono, ou tripanossomíase africana, é uma enfermidade negligenciada que afeta principalmente regiões da África subsaariana. Embora campanhas recentes tenham reduzido sua incidência, a doença ainda representa uma ameaça em áreas rurais, onde o controle da mosca tsé-tsé é limitado.
Os novos achados podem ter implicações diretas para estratégias de controle. Se formas slender também são transmissíveis, abordagens focadas exclusivamente em bloquear a diferenciação para o estágio stumpy podem ser insuficientes.
“Isso sugere que precisamos reconsiderar os alvos terapêuticos e os modelos epidemiológicos”, afirma Engstler. “A transmissão pode ser mais resiliente do que imaginávamos.”
Apesar da robustez metodológica, o estudo reconhece que algumas questões permanecem. Parte da comunidade científica ainda discute como definir precisamente uma célula slender e até que ponto os resultados podem variar entre diferentes cepas do parasita.
Ainda assim, o trabalho reforça uma mudança de perspectiva: o ciclo de vida do Trypanosoma brucei não é linear nem rigidamente definido, mas marcado por uma plasticidade inesperada.
“Talvez o mais importante seja reconhecer que a biologia desses parasitas é mais flexível do que pensávamos”, concluem os autores .
Para a ciência, trata-se de uma revisão conceitual significativa. Para a saúde pública, pode ser o início de uma nova abordagem no combate a uma das doenças tropicais mais persistentes do planeta.
Referência
Carina Praisler, Jaime N Lisack, Anna Sophie Kreis, Laura Hauf, Johanna Krenzer, Fabian Imdahl, Markus Engstler. Plasticidade inesperada no ciclo de vida do Trypanosoma brucei eLife 14 : RP108688. https://doi.org/ 10.7554/eLife.108688.2