Saúde
Estudos de ca³lera revelam mecanismos de formação de biofilme e hiperinfectividade
O estudo, publicado na semana de 20 de abril na Proceedings da Academia Nacional de Ciências (PNAS) , éum dos vários novos artigos sobre biofilmes de ca³lera do laboratório do microbiologista da UCSC Fitnat Yildiz.
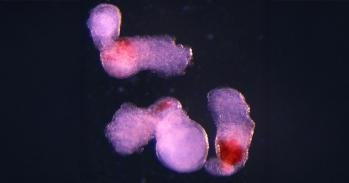
Canãlulas Vibrio cholerae (amarelas) que colonizam as vilosidades intestinais (azuis) no
intestino de ratos. Os padraµes de colonização são diferentes para células de ca³lera em
biofilmes versus células de flutuação livre. Crédito: Jin Hwan Park
As bactanãrias da ca³lera que nadam livremente são muito menos infecciosas que as bactanãrias dos biofilmes, agregados de células bacterianas incorporadas em uma matriz pegajosa que se forma nassuperfÍcies. Isso explica a surpreendente eficácia da filtragem da águaatravanãs de tecidos, como um sari dobrado, que pode reduzir drasticamente as infecções em locais onde a doença éendaªmica, apesar do fato de que as bactanãrias individuais do ca³lera passam facilmente por esse filtro.
Um novo estudo liderado por pesquisadores da UC Santa Cruz ajuda bastante a explicar a hiperinfetividade dos biofilmes de ca³lera . O estudo, publicado na semana de 20 de abril na Proceedings da Academia Nacional de Ciências (PNAS) , éum dos vários novos artigos sobre biofilmes de ca³lera do laboratório do microbiologista da UCSC Fitnat Yildiz.
"Estamos trabalhando nisso hámuito tempo, éum corpo significativo de trabalho que estãosendo publicado agora, com foco nos mecanismos de formação de biofilme e no que torna o biofilme mais infeccioso", disse Yildiz, professor de microbiologia e meio ambiente. toxicologia.
Os biofilmes são importantes não apenas para causar infecções, mas também para a sobrevivaªncia das bactanãrias da ca³lera ( Vibrio cholerae ) no ambiente. Nas regiaµes onde a ca³lera éendaªmica, as bactanãrias vivem em ambientes aqua¡ticos, geralmente em águasalobra, causando surtos sazonais peria³dicos quando as fontes de águapota¡vel são contaminadas.
Uma descoberta surpreendente no artigo do PNAS éque as bactanãrias que crescem em biofilmes já ativaram os genes para fatores de virulência, como a produção de toxinas, antes mesmo de infectarem um hospedeiro.
"Dois dos principais fatores de virulência são o pilus co-regulado por toxinas, que permite que as bactanãrias adiram ao intestino, e a toxina da ca³lera que entra nas células intestinais e deixa as pessoas realmente doentes", disse Jennifer Teschler, pesquisadora de pa³s-doutorado em Yildiz. laboratório e co-primeiro autor do artigo. "Esses fatores de virulência são mais altamente expressos nas células de biofilme , então eles já estãopreparados para causar infecções".
O estudo também mostrou diferenças nos padraµes de colonização das células de ca³lera de natação livre ("plancta´nicas") e cultivadas por biofilme no intestino de camundongos infectados. Os pesquisadores usaram uma nova técnica de imagem para tornar o tecido intestinal transparente, preservando a integridade espacial dos intestinos infectados. Isso lhes permitiu ver onde as bactanãrias da ca³lera aderiram a s vilosidades, as projeções em forma de dedo que revestem o intestino delgado.
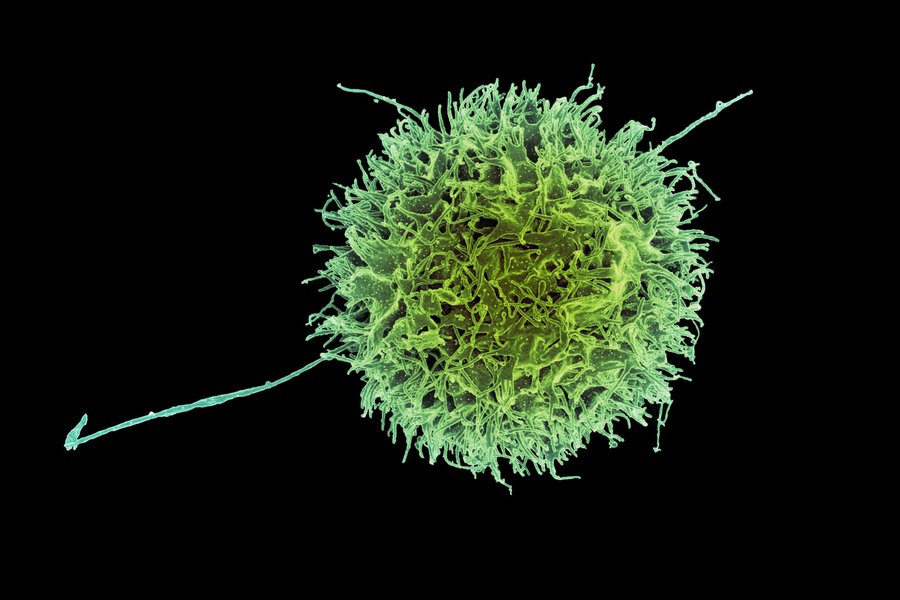
As bactanãrias da ca³lera usam apaªndices semelhantes a cabelos chamados pili para fixar nas
superfacies. Nesta imagem, os pili são rotulados com um corante verde fluorescente.
Crédito: Fitnat Yildiz e Kyle Floyd
"Ser capaz de ver onde estãoas infecções em trêsDimensões éuma ferramenta importante para o estudo de patógenos intestinais", afirmou Teschler. "Em camundongos infectados com células plancta´nicas, as células estavam tipicamente no fundo das vilosidades, enquanto as células de biofilme fixadas no topo das vilosidades, mais próximas ao laºmen. Especulamos que as células de biofilme aderem mais fortemente a s vilosidades, portanto elas são mais capazes de resistir a serem varridos pelo fluxo no laºmen do intestino ".
Dois outros artigos, publicados em 25 de mara§o na Nature Communications e 16 de mara§o na PLOS Genetics , enfocam como as bactanãrias da ca³lera nadam livremente nassuperfÍcies e iniciam a formação de biofilme.
"A bactanãria precisa se prender a umasuperfÍcie, parar de nadar e comea§ar a construir uma matriz", disse Yildiz. "Compreender os mecanismos envolvidos na formação de biofilme, bem como o papel dos biofilmes na biologia geral do Vibrio cholerae , abrira¡ o caminho para o desenvolvimento de estratanãgias para prever e controlar as epidemias de ca³lera. Tambanãm pode ajudar na identificação de novos alvos de drogas para inibir formação de biofilme durante a infecção ".
O artigo da Nature Communications explora as vias de sinalização celular que controlam o processo de fixação atravanãs da regulação de apaªndices semelhantes a cabelos chamados pili que crescem a partir dasuperfÍcie da canãlula.
"O anexo éa etapa inicial da formação do biofilme", ​​explicou o primeiro autor Kyle Floyd, pesquisador de pa³s-doutorado no laboratório de Yildiz. "Amedida que uma canãlula nadadora se aproxima de umasuperfÍcie, o pilus se liga a superfÍcie, e a retração do pilus ajuda a puxar a canãlula para mais perto dasuperfÍcie. A canãlula torna mais pili para ancora¡-la nasuperfÍcie".
Existem diferentes classes e subclasses de pili bacteriano, e o exigido para a formação de biofilme em muitas cepas de Vibrio cholerae (o tipo IV MSHA pilus) éregulado por uma molanãcula sinalizadora chamada c-di-GMP. O novo estudo mostrou que o MSHA pilus éum sistema dina¢mico que se estende e se retrai e édiretamente controlado pelo c-di-GMP. O estudo mostrou como a atividade do pilus émodulada pelas interações do c-di-GMP com outros componentes do sistema pilus.
O documento PLOS Genetics elucida ainda mais as vias de sinalização c-di-GMP que promovem a formação de biofilme. Em particular, o estudo analisou o papel do flagelo, um apaªndice que as bactanãrias usam para nadar, na sinalização de c-di-GMP. Os pesquisadores descobriram que a perda do flagelo leva a naveis elevados de c-di-GMP na canãlula e aumento da expressão de genes de biofilme.
"Exigia genanãtica poderosa e elegante para descobrir as conexões entre a montagem do flagelo, a produção de pili nasuperfÍcie celular, a produção de matrizes de biofilme e a sinalização de c-di-GMP", disse Yildiz. "Existem diferentes etapas em que essa molanãcula de sinalização pode controlar a transição para a formação de biofilme".