Tecnologia Científica
Elétrons revelam os segredos das moléculas
Estudo liderado por cientistas britânicos e japoneses cria método inédito para medir fatores de espalhamento atômico por criomicroscopia eletrônica e promete transformar a biologia estrutural, a química e o desenvolvimento de medicamentos
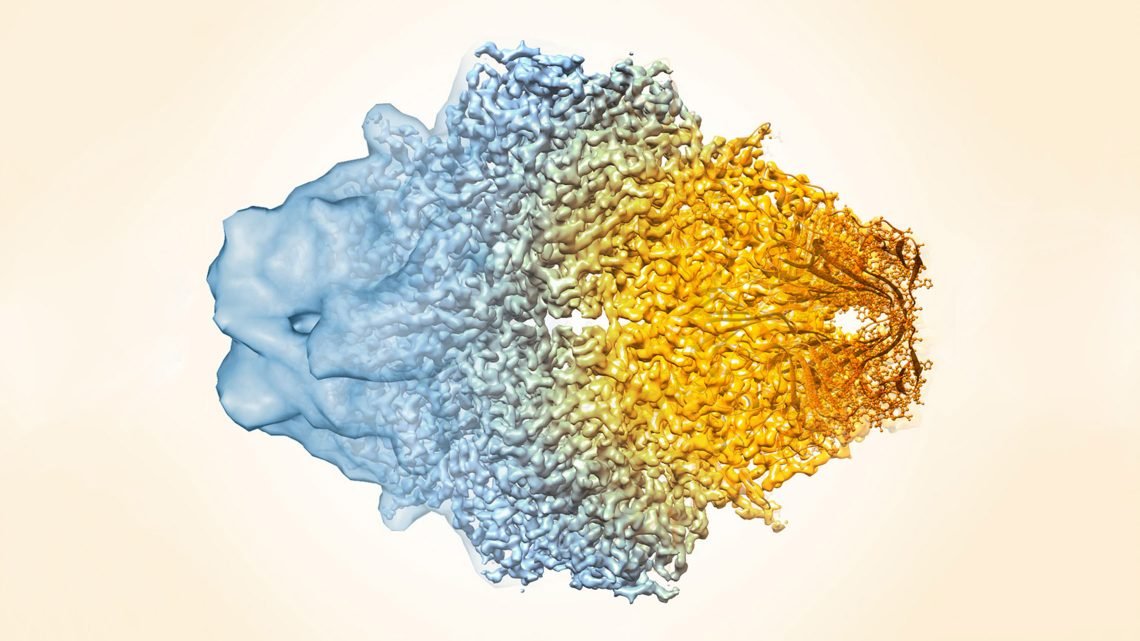
Imagens em cryo-EM passaram de bolhas irregulares para modelos que exibem átomos individuais, como neste vírus Zika. Foto de Illustration by ROYAL SWEDISH ACADEMY OF SCIENCES
Durante décadas, a criomicroscopia eletrônica — conhecida como cryo-EM — foi celebrada como uma revolução silenciosa da biologia molecular. A técnica, capaz de congelar proteínas em temperaturas extremas e revelar suas estruturas quase átomo por átomo, já ajudou a desvendar vírus, enzimas e mecanismos celulares antes invisíveis. Agora, um novo estudo internacional amplia ainda mais esse horizonte: pesquisadores conseguiram medir, com precisão inédita, como os elétrons se espalham ao redor dos átomos dentro de moléculas biológicas reais, incorporando efeitos químicos ignorados pelos modelos tradicionais há mais de meio século.
Publicado nesta sexta-feira (8), na revista científica Proceedings of the National Academy of Sciences (PNAS), o trabalho reúne cientistas do MRC Laboratory of Molecular Biology, da The University of Tokyo e da empresa Global Phasing Limited. A pesquisa foi liderada por Alexander Shtyrov, Richard Henderson e Garib N. Murshudov. Henderson é uma figura histórica na área: recebeu o Nobel justamente por desenvolver a criomicroscopia eletrônica aplicada a biomoléculas.
O estudo parte de uma constatação antiga, mas pouco resolvida: os modelos usados hoje para interpretar imagens de cryo-EM tratam os átomos como esferas neutras e isoladas, ignorando o impacto das ligações químicas e da redistribuição de cargas elétricas dentro das moléculas. Na prática, isso significa que proteínas complexas vêm sendo reconstruídas com aproximações consideradas “simplistas” pelos próprios autores.
“Compreender a estrutura das biomoléculas é essencial para explicar sua função”, escrevem os pesquisadores no artigo. Segundo eles, a distribuição eletrostática de uma molécula contém informações cruciais sobre posições atômicas e sobre como os elétrons são reorganizados pelas ligações químicas. Até agora, porém, modelar esses efeitos exigia cálculos computacionais proibitivos.
A equipe propôs uma solução baseada em inferência bayesiana e aprendizado de máquina. Em vez de depender exclusivamente de cálculos teóricos, os cientistas treinaram um modelo diretamente em mapas experimentais produzidos por cryo-EM. O algoritmo foi alimentado com reconstruções de alta resolução de enzimas catalase e dezenas de estruturas depositadas no banco internacional EMDB.
O resultado impressionou até os próprios autores. Os chamados “fatores de espalhamento empíricos” — parâmetros que descrevem como os elétrons interagem com os átomos — mostraram concordância muito superior com os dados experimentais. Em determinadas faixas de resolução, a variância do sinal não explicado caiu quase três vezes em comparação com os modelos clássicos usados atualmente.
“Estamos melhorando a forma como a microscopia eletrônica interpreta a matéria”, afirmou Garib N. Murshudov no artigo. Segundo ele, o novo método permite capturar características químicas reais das moléculas sem sacrificar velocidade computacional — um requisito indispensável para análises de proteínas gigantescas.
Os pesquisadores observaram especialmente mudanças importantes em grupos químicos sensíveis, como os carboxilatos presentes nos aminoácidos ácido aspártico e glutâmico. Essas regiões costumam sofrer danos induzidos pelo feixe de elétrons durante os experimentos, fenômeno conhecido como “decarboxilação”. O novo modelo conseguiu distinguir parte desses efeitos e reproduzir com maior fidelidade o comportamento eletrônico dessas estruturas.
A pesquisa também dialoga com uma longa tradição da física e da cristalografia. Desde os trabalhos pioneiros de Niels Bohr e Hans Bethe sobre espalhamento eletrônico, cientistas tentam descrever matematicamente como elétrons interagem com a matéria. Os modelos utilizados atualmente em cryo-EM derivam de aproximações desenvolvidas nas décadas de 1930 e 1950. O novo estudo sugere que essas bases começam a ser superadas pela combinação entre imagens ultrarrápidas, algoritmos bayesianos e inteligência computacional.
Veronica Falconieri, Subramaniam Lab, CCR, NCI, NIH
Além do impacto conceitual, os autores destacam aplicações práticas imediatas. Uma delas é o refinamento estrutural de proteínas usadas no desenvolvimento de medicamentos. Pequenas diferenças na distribuição eletrônica podem alterar a interpretação de sítios ativos, regiões de ligação e movimentos moleculares associados a doenças.
Outra consequência importante envolve a chamada “template matching”, técnica usada para localizar proteínas específicas dentro de imagens complexas de células congeladas. Segundo os pesquisadores, modelos eletrônicos mais precisos aumentam a correlação entre estruturas simuladas e imagens reais, tornando moléculas difíceis mais detectáveis.
O trabalho também abre portas para investigações sobre danos por radiação em biomoléculas. Os cientistas observaram que parte das anomalias vistas em proteínas pode não refletir apenas carga elétrica, mas também destruição química provocada pela própria microscopia. Para contornar esse problema, eles defendem experimentos com doses menores de elétrons e bancos de dados ainda maiores.
“Há necessidade de estruturas de resolução mais alta e com muito menos dano por radiação”, escrevem os autores.
A comunidade científica vê o avanço como parte de uma nova etapa da chamada “revolução da resolução”. Desde 2014, quando a revista Science popularizou a expressão “resolution revolution”, a cryo-EM passou de técnica marginal a ferramenta central da biologia estrutural. Em 2017, o Nobel de Química foi concedido a Richard Henderson, Joachim Frank e Jacques Dubochet por tornar possível visualizar biomoléculas congeladas em resolução atômica.
Agora, o novo estudo sugere que a próxima revolução talvez não venha apenas de microscópios mais poderosos, mas da maneira como os dados são interpretados.
Para especialistas da área, isso pode alterar desde pesquisas fundamentais sobre proteínas humanas até o desenho de antivirais, enzimas industriais e materiais nanoestruturados. A capacidade de representar com fidelidade o potencial eletrostático das moléculas é considerada crucial para entender processos químicos e biológicos em escala atômica.
Ao unir física quântica, biologia estrutural e aprendizado estatístico, o trabalho aponta para um cenário em que a microscopia eletrônica deixa de ser apenas uma ferramenta de visualização e passa a funcionar como um instrumento capaz de medir propriedades eletrônicas fundamentais da matéria viva.
Um detalhe aparentemente técnico, mas que pode redefinir a forma como a ciência enxerga o interior das moléculas.
Referência
UM.Shtyrov, H.Wilson, D.Slowik, K.Yamashita, J.Li,M.Wojdyr, S.Chen, G.McMullan, J.M.Curto, C.J.Russo, R.Henderson, & G.N.Murshudov, Medição de fatores de dispersão atômica por microscopia crioeletrônica, Proc. Natl. Acad. Sci. USA 123 (19) e2528758123, https://doi.org/10.1073/pnas.2528758123 (2026).